कार्बन मोनोअक्साइड
कार्बन मोनोअक्साइड (रासायनिक सूत्र: CO) एक विषाक्त, ज्वलनशील ग्यास हो। यो रंगहीन, गन्धहीन, स्वादहीन र हावा भन्दा थोरै कम घना हुन्छ। कार्बन मोनोअक्साइडमा एउटा कार्बन अणु र एउटा अक्सिजन अणु ट्रिपल बन्डद्वारा जोडिएका हुन्छन्। यो सबैभन्दा सरल कार्बनको अक्साइड हो। कोअर्डिनेसन कम्प्लेक्समा, कार्बन मोनोअक्साइड लिग्यान्डलाई कार्बोनिल भनिन्छ। यो औद्योगिक रसायनमा धेरै प्रक्रियाहरूमा एक प्रमुख अंश हो ।
| कार्बन मोनोअक्साइड | |
|---|---|

|

|
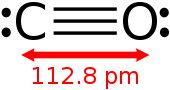
| |
Carbon monoxide | |
Other names Carbonic oxide gas Carbon protoxide Oxide of carbon Protoxide of carbon Carbonous oxide Carbonous acid gas Carbon(II) oxide Breath of carbon Oxygenated carbon Carbate Carbonyl Water gas Hydrocarbon gas Fuel gas Rauchgas Carbonic inflammable air Heavy inflammable air White damp Fire Damp Powder Gas Illuminating gas Dowson gas Mond gas Power gas Producer gas Blast furnace gas Coal gas Phlogiston Car gas | |
| Identifiers | |
| CAS number | 630-08-0 |
| PubChem | 281 |
| ChemSpider | 275 |
| UNII | 7U1EE4V452 |
| EC number | 211-128-3 |
| UN number | 1016 |
| KEGG | D09706 |
| MeSH | Carbon+monoxide |
| ChEBI | CHEBI:17245 |
| ChEMBL | CHEMBL1231840 |
| RTECS number | FG3500000 |
| Beilstein Reference | 3587264 |
| Gmelin Reference | 421 |
| Jmol-3D images | Image 1 |
| |
| |
| Properties | |
| Molecular formula | CO |
| Molar mass | 28.01 g mol−1 |
| Appearance | Colorless |
| Density |
|
| Melting point |
−205.02 °C, 68 K, -337 °F |
| Boiling point |
−191.5 °C, 82 K, -313 °F |
| Solubility in water | 27.6 mg/L (25 °C) |
| Solubility | soluble in chloroform, acetic acid, ethyl acetate, ethanol, ammonium hydroxide, benzene |
| Refractive index (nD) | 1.0003364 |
| Dipole moment | 0.122 D |
| Hazards | |
| Main hazards | Poisonous by inhalation[१] |
| NFPA 704 | |
| Explosive limits | 12.5–74.2% |
| Related compounds | |
| Other cations | Silicon monoxide Germanium monoxide Tin(II) oxide Lead(II) oxide |
| Except where noted otherwise, data are given for materials in their standard state (at 25 °C, 100 kPa) | |
| Infobox references | |
कार्बन मोनोअक्साइडको सबैभन्दा सामान्य स्रोत कार्बन युक्त यौगिकहरूको आंशिक दहन हो। धेरै वातावरणीय र जैविक स्रोतहरूले पनि कार्बन मोनोअक्साइड उत्पादन गर्छन्। उद्योगमा, कार्बन मोनोअक्साइड औषधी, ड्रग्स, सुगन्ध, र ईन्धन सहित धेरै यौगिकहरूको उत्पादनको लागि महत्त्वपूर्ण छ।[३] वायुमण्डलमा उत्सर्जन भएपछि, कार्बन मोनोअक्साइडले जलवायु परिवर्तन योगदान पुर्याउने धेरै प्रक्रियाहरूलाई असर गर्छ।[४]
भौतिक र रासायनिक गुणहरू
सम्पादन गर्नुहोस्प्रदुषण तथा स्वास्थ प्रभाव
सम्पादन गर्नुहोस्उत्पादन
सम्पादन गर्नुहोस्औद्योगिक उत्पादन
सम्पादन गर्नुहोस्कार्बन डाइअक्साइडको एक प्रमुख औद्योगिक स्रोत प्रड्युसर ग्याँस हो। प्रड्युसर ग्याँस कार्बन मोनोअक्साइड र नाइट्रोजनको मिश्रण हो, जुन कार्बनको अधिकता हुँदा उच्च तापक्रममा हावामा कार्बनको दहनबाट बनिन्छ। ओभनमा, हावालाई कोकबाट पार गरिन्छ।
सुरुमा उत्पादन गरिएको ढाँचा:CO2 ले तातो कार्बनसँग प्रतिकृया गरी CO बन्छ।[५] कार्बनसँग कार्बनडाइअक्साइडको प्रतिक्रियालाई बौडोअर्ड प्रतिक्रियाको रूपमा वर्णन गरिएको छ।[६] ८००°C भन्दा माथि, CO प्रमुख उत्पादन होः
ढाँचा:CO2 CO2 (g) + C (s) → 2 CO (g) (ΔHr = 170 kJ/mol)
अर्को स्रोत "वाटर ग्याँस" हो। वाटर ग्याँस भनेको हाइड्रोजन र कार्बन मोनोअक्साइडको मिश्रणहो। वाष्प र कार्बनको एन्डोथर्मिक प्रतिक्रियाको माध्यमबाट उत्पादन हुन्छ।
H2O (g) + C (s) → H2 (g) + CO (g) (ΔHr = 131 kJ/mol)
प्राकृतिक ग्याँस र अन्य इन्धनहरूबाट अन्य समान "सिन्थेसिस ग्याँस" प्राप्त गर्न सकिन्छ।
प्रयोग
सम्पादन गर्नुहोस्रासायनिक उद्योग
सम्पादन गर्नुहोस्धातु विज्ञान
सम्पादन गर्नुहोस्लेजर
सम्पादन गर्नुहोस्कार्बन मोनोअक्साइडलाई उच्च-शक्ति इन्फ्रारेड लेजरमा लेसिङ माध्यमको रूपमा पनि प्रयोग गरिएको छ।[७]
मंगल ग्रहमा इन्धनको रूपमा प्रस्तावित प्रयोग
सम्पादन गर्नुहोस्कार्बन मोनोअक्साइडलाई मंगल ग्रहमा इन्धनको रूपमा प्रयोग गर्ने प्रस्ताव गरिएको छ।
कार्बन मोनोअक्साइड/अक्सिजन इन्जिन प्रारम्भिक सतह यातायात प्रयोगको लागि सुझाउ दिइएको छ किनकि कार्बन मोनोअक्साइड र अक्सिजन दुबैलाई मंगल ग्रहको कार्बन डाइअक्साइड वातावरणबाट जिरकोनिया इलेक्ट्रोलिसिसद्वारा उत्पादन गर्न सकिन्छ, कुनै पनि मंगल जल स्रोतहरू प्रयोग नगरी हाइड्रोजन प्राप्त गर्न, जुन मिथेन वा कुनै पनि हाइड्रोजन-आधारित ईन्धन बनाउन आवश्यक पर्दछ।[८]
जैविक र शारीरिक गुणहरू
सम्पादन गर्नुहोस्फिजियोलोजी
सम्पादन गर्नुहोस्चिकित्सा
सम्पादन गर्नुहोस्माइक्रोबायोलोजी
सम्पादन गर्नुहोस्खाद्य विज्ञान
सम्पादन गर्नुहोस्विषाक्तता
सम्पादन गर्नुहोस्हतियारकरण
सम्पादन गर्नुहोस्प्राचीन इतिहासमा, ह्यानिबलले दोस्रो प्युनिक युद्धको समयमा कोइला धुवाँले रोमन कैदीहरूलाई मृत्युदण्ड दिए।[९]
केही सफाया शिविरमा नरसंहार समयमा चेल्मोनोमा ग्यास भ्यानहरू सबैभन्दा उल्लेखनीय, र एक्शन टी४ "इच्छामृत्यु" कार्यक्रममा कार्बन मोनोअक्साइड प्रयोग गरिएको थियो।[१०]
सन्दर्भ सामग्रीहरू
सम्पादन गर्नुहोस्- ↑ उद्दरण त्रुटी: अवैध
<ref>चिनो;PGCHनामको सन्दर्भका लागि कुनै पाठ प्रदान गरिएको छैन - ↑ "Carbon Monoxide - CAMEO Chemicals", cameochemicals.noaa.gov, US NOAA Office of Response and Restoration।
- ↑ Ullmann's Encyclopedia of Industrial Chemistry।
- ↑ Voiland, Adam, "Fourteen years of carbon monoxide from MOPITT", Climate Change: Vital Signs of the Planet, अन्तिम पहुँच २०२२-०३-०४।
- ↑ "Carbon Monoxide", अन्तिम पहुँच २१ मे २०२१।
- ↑ Gasification, पृ: १२।
- ↑ Ionin, A.; Kinyaevskiy, I.; Klimachev, Y.; Kotkov, A.; Kozlov, A. (२०१२), "Novel mode-locked carbon monoxide laser system achieves high accuracy", SPIE Newsroom, डिओआई:10.1117/2.1201112.004016।
- ↑ Landis (२००१), "Mars Rocket Vehicle Using In Situ Propellants", Journal of Spacecraft and Rockets 38 (5): 730–735, डिओआई:10.2514/2.3739, बिबकोड:2001JSpRo..38..730L।
- ↑ Hopper, Christopher P.; Zambrana, Paige N.; Goebel, Ulrich; Wollborn, Jakob (२०२१-०६-०१), "A brief history of carbon monoxide and its therapeutic origins", Nitric Oxide (अङ्ग्रेजीमा), 111-112: 45–63, आइएसएसएन 1089-8603, डिओआई:10.1016/j.niox.2021.04.001, पिएमआइडी 33838343।
- ↑ A history of modern Germany, 1800–2000, पृ: ३२३।
